Nguyên tử là những hạt rất nhỏ, là các hạt cơ bản cấu thành nên các dạng vật chất. Hạt nhân nguyên tử chiếm gần như toàn bộ khối lượng trong cấu tạo nguyên tử. Vậy hạt nhân nguyên tử cấu tạo bởi những thành phần nào? Đây là câu hỏi trắc nghiệm thường xuyên xuất hiện trong các bài kiểm tra, hãy cùng imo2007 làm rõ vấn đề này nhé.

Hạt nhân nguyên tử được cấu tạo bởi?
A. Proton và nơtron.
B. Proton và electron.
C. Nơtron và electron.
D. Proton, nơtron và electron.
Đáp án đúng là A: Proton và Nơtron
Nguyên tử là đơn vị cơ bản cấu thành nên mọi vật chất và được sử dụng với mục đích xác định cấu trúc của các nguyên tố. Nguyên tử là những hạt có kích thước vô cùng nhỏ và trung hoà về điện. Cấu tạo của nguyên tử bao gồm một hạt nhân nặng mang điện tích dương ở trung tâm và xung quanh hạt nhân được bao bọc bởi đám mây điện tích âm được cấu thành bởi các hạt electron. Hạt nhân nguyên tử được tạo thành bởi 2 loại hạt chính là Proton và Nơtron, hạt proton mang điện tích dương, còn nơtron không mang điện.
Chính vì vậy hạt nhân nguyên tử được cấu tạo bởi proton và nơtron. Đáp án A là đáp án đúng.
Định nghĩa về hạt nhân nguyên tử
Hạt nhân nguyên tử có mật độ rất cao, có thể đạt đến 100 triệu tấn/cm3 và chiếm gần như toàn bộ khối lượng của nguyên tử. Theo các tài liệu hiện nay, kích thước của hạt nhân nguyên tử được giới hạn trong một phạm vi có bán kính khoảng 10^-15m.

Cấu tạo của hạt nhân nguyên tử bao gồm hai loại hạt chính:
Proton: từ tiếng Hy Lạp có nghĩa là “thứ nhất”, mang điện tích dương với khối lượng rất nhỏ, chỉ xấp xỉ 1.67262158 × 10^-27 kg (tương đương với 938.278 MeV/c2).
Nơtron: không mang điện tích và có khối lượng khoảng 1.67492716 × 10^-27 kg (tương đương với 939.571 MeV/c2), lớn hơn khối lượng của proton.
Một số kiến thức quan trọng xung quanh hạt nhân nguyên tử
Sau khi hiểu được hạt nhân nguyên tử cấu tạo bởi thành phần nào thì bản thân hạt siêu nhỏ này có nhiều lý thuyết rất quan trọng và thú vị khác.
Nguyên tố hoá học
Nguyên tố hóa học là các nguyên tử mà hạt nhân của chúng có cùng số điện tích (được biểu diễn bằng số nguyên tử Z). Hiện nay, khoa học đã xác định được sự tồn tại của 94 nguyên tố hóa học tự nhiên và con người đã tạo ra 24 nguyên tố khác từ các thí nghiệm hạt nhân, tổng cộng là 118 nguyên tố.

Nguyên tố Oxy là một ví dụ điển hình. Tất cả các nguyên tử với số nguyên tử Z là 8 đều thuộc về nguyên tố này. Điều này có nghĩa là chúng có 8 proton và 8 electron.
Số hiệu nguyên tử
Số hiệu nguyên tử chính bằng số đơn vị điện tích hạt nhân của nguyên tố đó. Số hiệu nguyên tử có ký hiệu là Z.
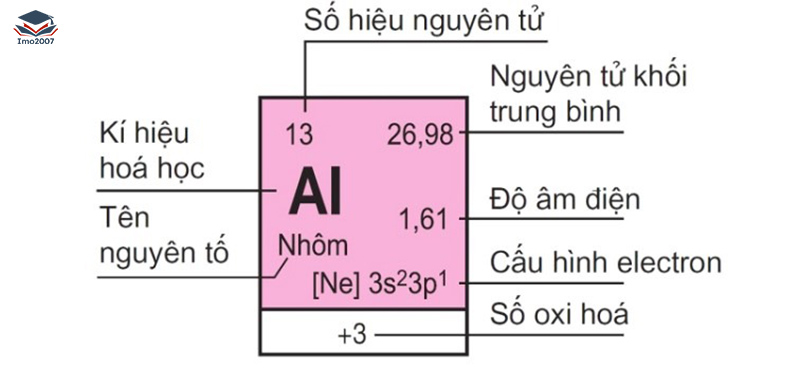
Ký hiệu nguyên tử
Các đặc điểm cơ bản nhất của nguyên tử là số nguyên tử (số proton trong hạt nhân) và số khối. Để biểu thị một nguyên tử, người ta thường sử dụng các chỉ số đặc trưng được đặt bên trái của ký hiệu nguyên tố X, trong đó số khối (biểu thị bằng A) nằm phía trên và số nguyên tử (biểu thị bằng Z) nằm phía dưới.
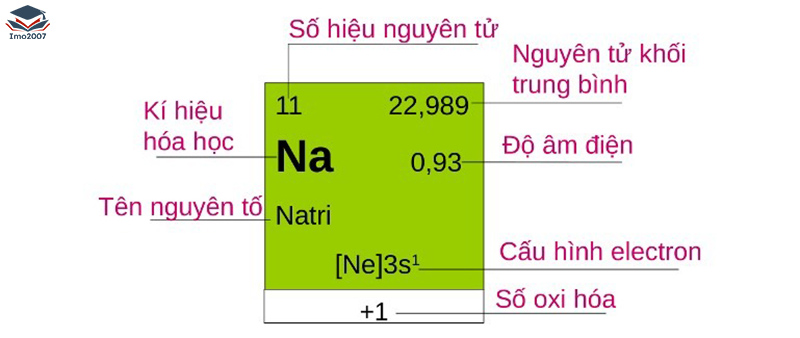
Ví dụ, trong hình minh họa, chúng ta thấy rằng nguyên tử của Natri có số khối là 23 và số nguyên tử là 11. Từ đó, ta có thể suy luận rằng số nguyên tử của Na là 11 (bao gồm 11 proton và 11 electron, vì hạt nhân trung hoà về điện nên số proton = electron), và trong hạt nhân có tổng cộng 12 neutron (bằng số nguyên tử trừ đi số khối).
Đồng vị
Các nguyên tử có cùng điện tích không phải lúc nào cũng có khối lượng bằng nhau. Nguyên nhân chính của hiện tượng này là do mỗi nguyên tử, mặc dù có cùng số proton, nhưng lại có số nơtron khác nhau trong hạt nhân. Các đồng vị của các nguyên tố hóa học có cùng số proton nhưng khác nhau về số nơtron, chúng được phân loại vào cùng một ô trên bảng tuần hoàn nguyên tố hóa học. Vì số nơtron khác nhau, số khối của các đồng vị sẽ thay đổi tương ứng. Tóm lại, đồng vị là những nguyên tử có cùng số proton, electron nhưng khác nhau về số nơtron.
Ví dụ: Nguyên tố Hidro có 3 đồng vị như sau:
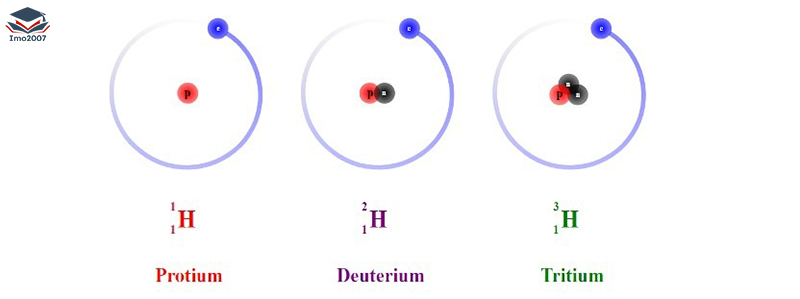
Nguyên tử khối
Nguyên tử khối, hay còn gọi là khối lượng nguyên tử tương đối của một nguyên tử. Khối lượng của một nguyên tử được tính bằng tổng khối lượng của proton và nơtron trong hạt nhân, cộng thêm khối lượng của electron. Tuy nhiên, vì khối lượng của electron quá nhỏ so với proton và nơtron, nên thông thường khối lượng của một nguyên tử được coi xấp xỉ bằng khối lượng hạt nhân của nguyên tử đó.
Do đó, khối lượng nguyên tử được hiểu chính là số khối (A). Chẳng hạn, nguyên tử khối của Photpho (P) có N = 16 và Z = 15. Vậy nguyên tử khối = 16 + 15 = 31
Nguyên tử khối trung bình
Vì ở trong tự nhiên, có rất nhiều nguyên tố hóa học tồn tại với nhiều đồng vị nên nguyên tử khối được tính bằng nguyên tử khối trung bình của các đồng vị đó.
Chẳng hạn có một nguyên tố có 2 đồng vị X và Y, X là nguyên tử khối tương ứng của đồng vị X và Y tương ứng là nguyên tử khối của đồng vị Y, a là phần trăm số nguyên tử của X và b là phần trăm số nguyên tử của Y. Từ đó, công thức tính nguyên tử khối trung bình của A là: (aX + bY)/100
Như vậy, thông qua bài viết này, các em đã nắm được hạt nhân nguyên tử cấu tạo bởi những thành phần nào cũng như hiểu hơn một số kiến thức xung quanh hạt nhân nguyên tử. Chúc các em học tốt môn Hoá.
Xem thêm: Chất điện li là gì? Phân loại chất điện li mạnh và yếu trong hoá học